Fundamentos de Física
E quanto às energias das órbitas eletrônicas?
Suponhamos que queremos medir não apenas a energia de uma partícula, mas também a duração do intervalo de tempo que ela permanece com esta energia. A relação de incerteza de Heisenberg:
em que e são, respectivamente, as incertezas na energia e no intervalo de tempo, impõe uma revisão no conceito de estado estacionário. Nesta relação, é a constante de Planck dividida por .
Consideremos que um elétron passa da órbita 1, correspondente ao estado fundamental do átomo, para a órbita 2, correspondente ao primeiro estado excitado do átomo. O elétron permanece na órbita 2 certo intervalo de tempo e depois retorna à órbita 1. O intervalo médio de tempo durante o qual o elétron permanece na órbita 2, chamado de vida média do estado correspondente, não pode ser previsto. Na verdade, só podemos falar na probabilidade por unidade de tempo de que o elétron salte ao estado de menor energia. Desse modo, o intervalo de tempo médio durante o qual o elétron permanece no estado excitado, que é inversamente proporcional à dita probabilidade, só pode ser conhecido com certa imprecisão . Assim, a grandeza , dada por:
pode ser considerada como a imprecisão com que podemos determinar o valor da energia do estado excitado em questão. A grandeza é chamada de largura de energia do estado considerado. Medidas da energia do estado excitado dão, com maior probabilidade, valores entre (½) e (½).
De modo geral, uma boa estimativa para o valor máximo de é supor que ele seja da ordem de , a vida média do estado:
Desse modo, quanto maior a vida média de um estado, menor é a correspondente largura de energia.
A vida média do estado fundamental é infinita porque um átomo, nesse estado, não pode realizar uma transição para um estado de energia menor. Assim, para o estado fundamental, . Em palavras: a energia do estado fundamental pode ser determinada exatamente.
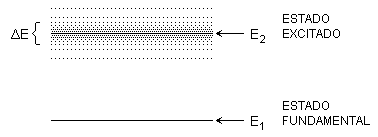
Qualquer outro estado deve ter uma largura de energia diferente de zero. Por isso, a energia emitida numa transição radiativa não é bem definida. Numa transição entre os estados de energia (não necessariamente o estado fundamental) e , os fótons emitidos ou absorvidos têm energia entre os seguintes valores:
e
em que é a largura de energia total dos dois estados.
Para dar uma idéia da ordem de grandeza de , consideremos o primeiro estado excitado do átomo de mercúrio, cuja vida média é da ordem de . Com:
temos:
A energia do primeiro estado excitado do átomo de mercúrio é de . Portanto, é cerca de vezes menor do que .
Volte para Princípio de Incerteza de Heisenberg.
Site do Grupo de Ensino de Física da Universidade Federal de Santa Maria (GEF-UFSM)